※当ホームページに掲載されている文書、画像等の無断転載・無断引用は禁止とさせていただきます。
文字
背景
行間
日誌
化学実験~再結晶~
2年生の化学の授業で再結晶の実験をおこないました。再結晶とはより純度の高い結晶を得る精製法。純度の低い結晶を水などの溶媒に溶かし、その溶媒の蒸発や温度差による溶解度(溶媒に溶けることのできる限界量)の違いを利用する精製法です。今回の実験では硝酸カリウムを用いた再結晶をおこない、析出した結晶を観察しました。
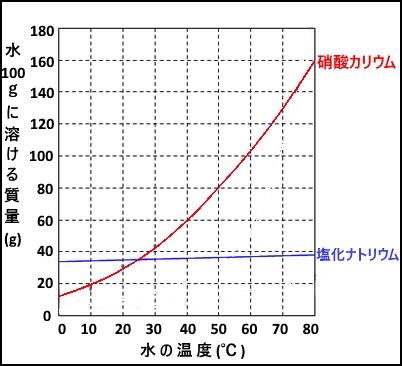
上のグラフが硝酸カリウムと塩化ナトリウムの溶解度曲線です。硝酸カリウムは水温変化に対する飽和量の変化が大きいので、飽和量の差を利用して短時間で多くの再結晶を析出させることができます。硝酸カリウムと水を試験管に入れ加熱溶解し、その後冷却して再結晶の様子を観察しました。

写真のように水を入れた直後は硝酸カリウムは溶けきらず、試験管の底に粉末状態で残っています。加熱していくと溶解度が上がり溶解が進み、加熱を続けると全て溶解します。

写真は加熱後の試験管を水で冷却しているところです。溶液温度が低下すると、溶解していた硝酸カリウムが試験管の底に結晶として析出してきます。溶かす前の白い粉末とは違い、やや透き通った針状の結晶となります。結晶形態は物質により色や形状が異なります。今回は授業内でおこなう実験で速やかに冷却して結晶化したが、再結晶は時間をかけてゆっくり析出させると綺麗な形の結晶をつくることができます。

上のグラフが硝酸カリウムと塩化ナトリウムの溶解度曲線です。硝酸カリウムは水温変化に対する飽和量の変化が大きいので、飽和量の差を利用して短時間で多くの再結晶を析出させることができます。硝酸カリウムと水を試験管に入れ加熱溶解し、その後冷却して再結晶の様子を観察しました。

写真のように水を入れた直後は硝酸カリウムは溶けきらず、試験管の底に粉末状態で残っています。加熱していくと溶解度が上がり溶解が進み、加熱を続けると全て溶解します。

写真は加熱後の試験管を水で冷却しているところです。溶液温度が低下すると、溶解していた硝酸カリウムが試験管の底に結晶として析出してきます。溶かす前の白い粉末とは違い、やや透き通った針状の結晶となります。結晶形態は物質により色や形状が異なります。今回は授業内でおこなう実験で速やかに冷却して結晶化したが、再結晶は時間をかけてゆっくり析出させると綺麗な形の結晶をつくることができます。


















